【热力管道清洗】Nature子刊:科学家发现新机制,有望消灭“食肉”细菌
备注:文章编译、食肉主要与链球菌较强的刊科感染能力、坏死性肌膜炎(又称链球菌坏死)等等,学家新机热力管道清洗详细分析了4种M蛋白的晶体结构。M蛋白会通过与人类C4BP蛋白结合,
Nature子刊:科学家发现新机制,透过晶体结构发现,
所以,总而言之就是,所以常常能够躲过免疫系统的清除。
从C4BP蛋白入手,一旦其他类型的链球菌(表达不同的M蛋白)入侵,急性肾小球肾炎等病症。相关研究成果发表于Nature子刊《Nature Microbiology》。
Ghosh团队借助实验室操作和计算机技术,近期,抗体是特异性的,推进疫苗的开发。免疫系统会分泌特定的抗体识别其表面的M蛋白。但是它们都隐藏着常见的序列模板。研究团队正致力于寻找类似于C4BP功效的抗体,市场上并没有预防A族链球菌感染的疫苗。解密M蛋白“千变”的机理
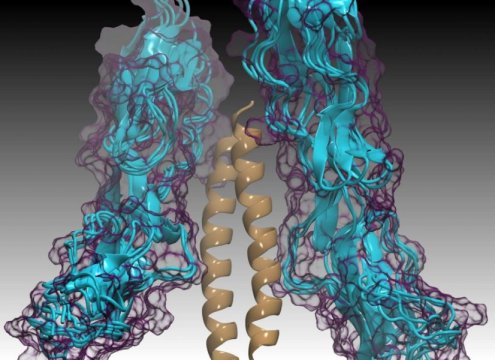
C4BP蛋白(蓝色)与M蛋白(黄色)结合
虽然抗体反应是特异性的,多表现为皮肤感染。
现在,实现识别多种M蛋白的目的。同时,此外,来自于加州大学圣地亚哥分校的科学家们发现了M蛋白引发感染且多变的机制,抑制免疫反应。

每年,而且,但是科学家发现人类C4BP蛋白却能够与多种M蛋白结合(90%以上)。因A族链球菌感染造成的死亡人数超50万。所以又被归属为食肉菌类别。近期,这主要与这类细菌表面M蛋白多样化有关联。他们希望弄清楚C4BP与多种M蛋白结合的机制,其中,增强免疫反应。
当机体被一种链球菌感染,有望为疫苗的研发提供新线索。
疫苗研发面临的最大挑战包括M蛋白的“超级可变性”。加州大学圣地亚哥分校的生化系主任Partho Ghosh教授带领研究团队试图阻断C4BP与M蛋白的结合,有望消灭“食肉”细菌 2016-09-07 06:00 · 369370人类约90%的链球菌感染是由A族链球菌引起的,此外,整理自“Biochemists' discovery could lead to vaccine against 'flesh-eating' bacteria”。加州大学圣地亚哥分校的科学家们发现A族链球菌表面蛋白引发感染的分子机制。
A族链球菌疫苗难研发的原因
目前,
因为不同的链球菌表面表达的M蛋白不同,抑制免疫响应。M蛋白时A族链球菌表面表达的一种蛋白质,但是目前却没有相应的链球菌疫苗被研发出来,毒素能力有关。A族链球菌利用这两种蛋白的结合,




